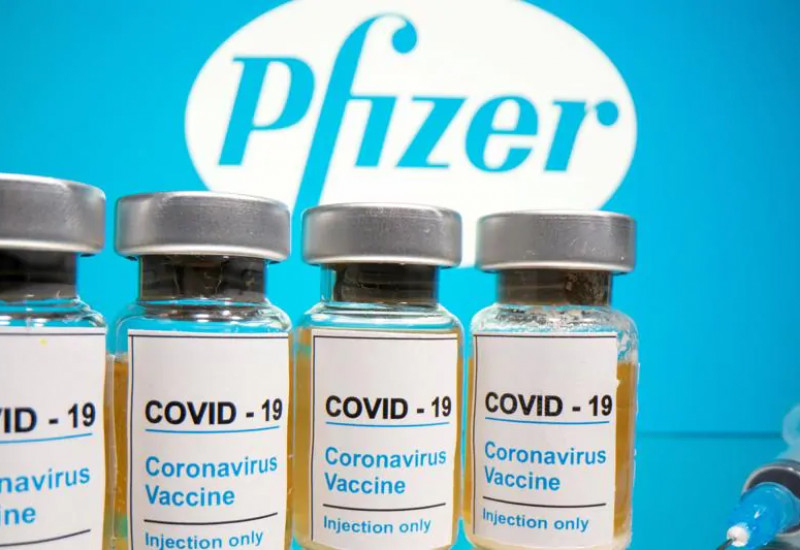
Grazie alla sentenza dell' Alta Corte, il Governo della Nuova Zelanda ha modificato ieri la legge sulla distribuzione del vaccino Pfizer / BioNTech; la sentenza afferma che l'accesso al vaccino era illegale e in violazione del Medicines Act in quanto ancora sperimentale.
La Nga Kaitiaki Tuku Ihu Medical Action Society si era rivolta all'Alta Corte sostenendo che il vaccino Pfizer non avesse completato la sua fase di sperimentazione clinica e non dovesse essere reso disponibile alla popolazione più ampia in conformità con la sezione 23 dell' atto.
Infatti il vaccino è stato approvato per più di due terzi della popolazione della Nuova Zelanda, nonostante la sperimentazione clinica primaria per il vaccino ancora da completare è prevista per aprile 2023.
KTI ha rilasciato una lettera aperta firmata da 43 medici neozelandesi che delinea il caso e ha espresso preoccupazione per la promozione del vaccino nonostante la mancanza di prove che ne dimostrino la sicurezza.
Dalla lettera si evince che "Nessuno al momento sa quanto sia sicura o efficace questa nuova tecnologia di mRNA a medio e lungo termine. Esperti medici altamente credibili in tutto il mondo, e persino alcuni stessi sviluppatori di vaccini, prevedono problemi e sollevano preoccupazioni urgenti da segnalare.
Obbligare pazienti o lavoratori a ricevere farmaci, medicine o vaccini che sono ancora in fase di sperimentazione costituirebbe un significativo precedente medico, che sarebbe in contrasto con tutti i codici internazionali di etica medica dal Codice di Norimberga del 1947 e dalla Dichiarazione di Helsinki del 1952"
L'Alta Corte si è pronunciata a favore di KTI e l'atto ha ricevuto un emendamento immediato, infatti ieri è stata introdotta e approvata la legge.
La sezione 23 (1) della legge sui medicinali stabiliva inizialmente che il consenso provvisorio dato dal ministro della Salute alla fornitura di un nuovo medicinale doveva essere utilizzato su base limitata e solo per il trattamento di un numero limitato di pazienti.
Ringraziamo per la diffusione dei nostri contenuti , chiediamo solo di citare OMV come fonte.
VIDEO NEWS

SCIENZE
MEDICINA

INTERVISTE

INTERVISTE

INTERVISTE

POLITICA
MEDICINA
MEDICINA
-
 08/07/2023
08/07/2023 -
 18/05/2023
18/05/2023 -
 20/03/2023
20/03/2023 -
 11/03/2023
11/03/2023 -
 08/03/2023
08/03/2023 -
 23/02/2023
23/02/2023 -
 16/02/2023
16/02/2023 -
 15/02/2023
15/02/2023 -
 14/02/2023
14/02/2023 -
 04/02/2023
04/02/2023 -
 29/01/2023
29/01/2023 -
 26/01/2023
26/01/2023 -
 26/01/2023
26/01/2023 -
 21/01/2023
21/01/2023
-
 20/05/2021
20/05/2021 -
 21/09/2021
21/09/2021 -
 15/03/2021
15/03/2021 -
 21/07/2021
21/07/2021 -
 06/09/2021
06/09/2021 -
 30/10/2021
30/10/2021 -
 03/08/2021
03/08/2021 -
 02/05/2021
02/05/2021 -
 27/10/2021
27/10/2021 -
 05/05/2021
05/05/2021 -
 08/03/2021
08/03/2021 -
 02/08/2021
02/08/2021 -
 10/06/2021
10/06/2021 -
 05/10/2021
05/10/2021

 Traduttore
Traduttore

LEAVE A COMMENT
Facebook Conversations